打通医疗器械产业化“最后一公里”中关村这个专业服务平台来了
2020-06-12 08:00:00source | 网络
在国内医疗器械行业,一直有“国货不强”的说法,特别是在高端医疗器械领域,国产与进口设备使用之比大约是1:9。
那么,国货是真的不强吗?
有人认为问题主要在于国货在技术上存在“先天不足”。其实不然,有一个关键环节一直没有得到国内研发企业的重视,那就是非功能性检测。
什么是非功能性检测?
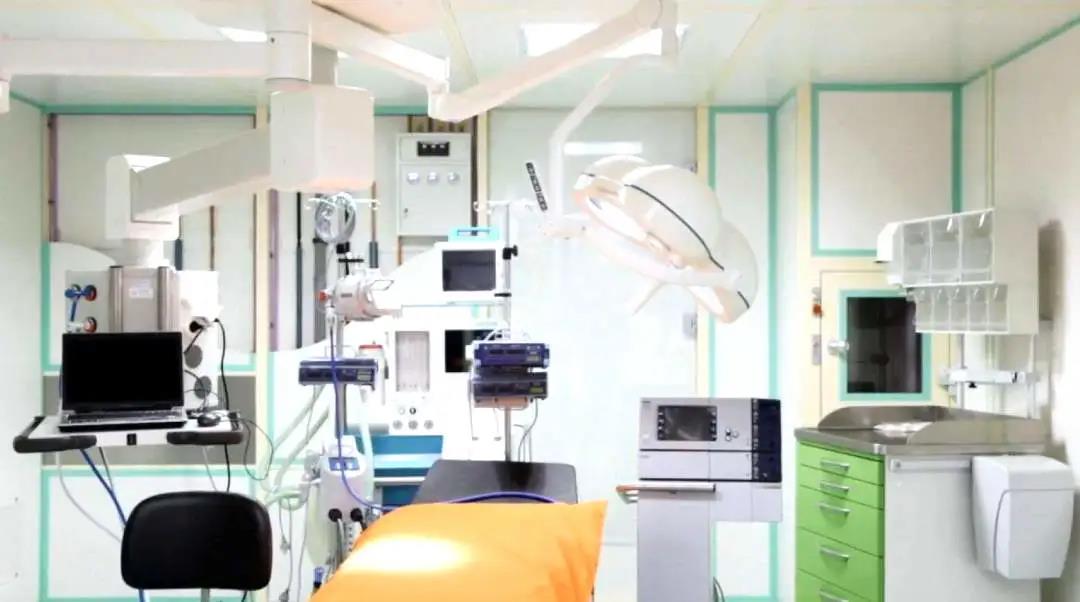
以呼吸机为例,作为一个医疗器械产品,呼吸机的主要功能就是实现机械通气。但这是远远不够的,在真正的临床应用中,呼吸机同时还要具备耐压、抗震、抗电磁干扰、防水防霉防粉尘等能力,这些就是呼吸机非功能性部分需要解决的问题。医疗器械好不好用、耐不耐用很大程度上是由产品的非功能性部分决定的。
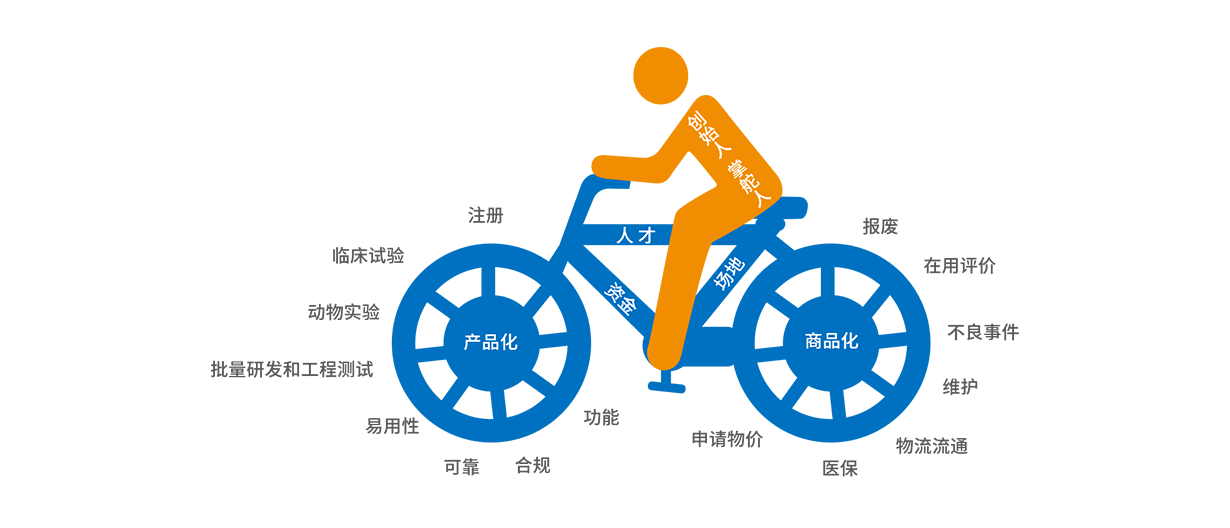
针对这个问题,中关村里有一家企业搭建了一个专业的、面向市场的检测实验室,专门为医疗器械研发企业提供市场空白的非功能性检测服务。这就是由北京中关村水木医疗科技有限公司打造的国内首个医疗器械全链条专业服务平台,专注为国产医疗器械产品“找找bug”,并提出专业的修改建议,让国货真正强大起来。 中关村水木医疗 北京中关村水木医疗科技有限公司成立于2017年,是在中关村管委会的指导下,由中关村发展集团、首科集团、中关村医疗器械园、水木东方等投资打造的全国首个医疗器械全链条服务平台,助力医疗器械研发企业加快推进临床、上市进程,解决创新医疗器械产业化、商业化“最后一公里”的难题,2019年4月被认定中关村高新技术企业,服务平台已纳入中关村示范区高精尖产业协同创新平台。 提前“体检” 量身打造合规的医疗器械 有人可能会问,为什么要建这样一个专业实验室?医疗器械产品在注册检验和技术审评阶段会经过同样的检验,企业再花钱进行专门检验,有必要吗? 以自行车为例打个比方,如果把医疗器械产品从研发到销售上市的产业链看作自行车的车轮,那么产品的功能性只能代表车轮的一部分,而合规、可靠、易用等非功能性就是其它组成部分,它们共同构成一个完整的产品,这样轮子才能转动起来。 医疗器械产业链示意图 无论是高、中、低端产品,国外的医疗器械企业普遍会对研发中的产品进行专业的非功能性检测,并依据检测结果进行相关提升整改,从而让产品更加易用、耐用。这就是很多人认为进口产品更“好用”的主要原因。 国产医疗器械性能方面并不输进口医疗器械,而当前市场上多采用进口产品,问题就出在国产医疗器械合规性、可靠性设计不够。 而之所以出现这个问题,水木医疗创始人孙京昇认为,主要原因是国内医疗器械研发企业缺少具备监管经验的相关人才,且在研发过程中缺乏对合规性、可靠性的把握,在医疗器械新产品进入注册、临床阶段后,问题就暴露出来了,临时按检测结果和技术审评意见修修补补,不仅导致研发周期加长,而且无法达到更高标准和临床使用要求。 针对这个行业痛点,拥有20年专业医疗器械监管工作经历的创始团队于2017年成立了水木医疗,以能够填补市场空白的医疗器械非功能性检测为核心,通过建立一站式综合服务,为医疗器械企业提供“医疗器械工程化设计+检验认证注册+临床CRO+垂直流通+基金”的一条龙服务。 水木医疗位于中关村亦庄园的总部内,建有面积达3600平方米的服务平台检测实验室。走进水木医疗的实验室,各式各样的检测设备可谓五花八门。在可靠性实验室,我们可以看到有一台重达10余吨的检测设备,外形看就像一段公路路面,能够模拟各种路面坡度,这台设备就是专门用来测试医疗器械在运输过程中外包装的安全性,看看在不同程度的路面环境下产品包装是否能够保持完整。还有一台设备专门用来模拟风沙天气,启动后里面就会刮沙尘暴,这台机器就是用来测试产品抗粉尘能力,看看医疗器械能不能在沙尘暴天气下正常工作。 电气安全实验室 这些检测设备不仅体积大,很多还需要从国外进口,一般的医疗器械研发企业很难自己配置专门的实验室进行检测。 现在,研发企业则可以将自己的产品送到水木医疗的检测实验室中,经过一系列“严苛的考验”后,能够提前发现问题,尽量避免“临时抱佛脚”。 不可或缺 为医疗器械打磨“筋骨” 对于一件医疗器械产品来说,“能用”和“好用”是两个完全不同的概念,而要想达到“好用”的水平,这里面是大有门道的。 很多研发中的产品在水木医疗进行全面“体检”后,能够“对症下药”,有针对性地对产品进行调整。 一台正在研发中的医疗设备正在水木医疗的实验室中进行电磁波检测。在正常情况下工作时,这台设备的电磁波动正常规律,但是如果周围出现功率大的设备,我们能够看到电磁波检测仪上出现了很明显的波动起伏,这就说明这台设备在电磁稳定性和可靠性上还需加强。 此前,一台用于精确治疗肿瘤的碳离子治疗设备送到水木医疗进行检测。这是国内第一台拥有自主知识产权的医用碳离子加速器,送到实验室的时候已基本完成功能部分的研发,但是由于设备上使用的数个子系统以及上万个零部件大部分均为自主研发生产,所以存在很多应用方面的问题,更无法满足医疗器械相关法律法规的要求。 经过水木医疗一整套专业检测和整改后,该产品不仅符合现有电气安全、电磁兼容性、软件安全等强制标准,产品的可靠性、临床性能和可用性也得到提升。目前该产品已顺利进入临床试验阶段。 水木医疗的检测整改CDO平台设有安全实验检测平台、医疗器械软件实验平台、可靠性平台、体外诊断研发测试平台、专业医疗器械研发测试平台等5个专业子平台,还拥有国内稀缺、技术领先的医疗器械专业电磁兼容实验室,包括三米法和十米法半电波暗室、屏蔽室和性能监测设备。 电磁兼容EMC实验室 “简单来说,产品在所有检测台上过一遍,将解决90%有源医疗器械的检验问题。国产高端医疗器械想要追赶国际水平,提升行业粘度,就一定要克服非功能化问题,让医疗器械产品能够经受任何考验。”水木医疗总经理黄文广说。 预计2020年中旬,5个子平台能完成实验室建设,最快年底取得CNAS(中国合格评定国家认可委员会)、CMA(中国计量认证)200项认证。 去伪存真 让研发企业少走回头路 水木医疗成立两年来,已经为上百家医疗器械研发企业提供咨询、指导服务,在协同创新过程中,让之前因种种原因停滞了的医疗器械研发项目重新进入快速研发轨道,并顺利通过注册检验提前进入临床阶段,帮企业节省上千万元费用。 “我们是把以前在医疗器械研发、注册、检验、临床和监管的技术和工作经验前移到企业新产品研发的全流程。”孙京昇说。 水木医疗在企业医疗器械新产品研发一开始,就全面跟进指导工程化设计、检验、认证、注册、临床试验研究。全程指导企业设计怎么做、各流程都有什么要求、需要留下什么资料、要做什么验证。杜绝在注册检验和技术审评阶段对医疗器械可靠性修修补补,提前“量体裁衣”,让研发的医疗器械真正成为可临床使用的可靠产品,快速通过注册检验、临床并上市。 医疗器械检测服务不断市场化是大势所趋。近年来,医疗器械检验业务正从相关部门指定检验机构的方式,转向开放第三方检验机构。 截至目前,水木医疗投资了5000多万元,不断完善检验和研发能力。已经建成医疗机器人实验室,并与全国1/3以上医疗机器人研发企业达成合作意向,不但在合规性、可靠性方面进行深度合作,在标准制定和测试方法研究方面也将深度合作。 未来三年,水木医疗除了完成1.1亿元的投资,不断提升和完善检验和研发能力之外,还把目光投向数据库建设,希望通过对检测经验的数据化、可视化,避免医疗器械研发企业出现共性问题,少走回头路,最终实现公司与研发企业的双赢。